
圖片來源:https://www.jiemian.com/article/506742.html
人生路上常常遇到分叉路口,在這個選擇的一瞬間我們的命運將會改變,選擇A,可能會成為制作舌尖上的美食的大廚;選擇B,可能成為此刻在電腦前碼代碼的我。
眾所周知,多能干細胞具有分化成不同類型的子細胞的多能性。而對于這些干細胞來說,在它分化的路上也會遇到“向左走”還是“向右走”的難題。此前大量的研究發現,這個選擇的關卡是由一些關鍵的轉錄因子調控的,但是這些轉錄因子如何決定干細胞的分化進程還并不完全清楚。 近年來,隨著計算生物學的發展特別是單細胞組學的迅猛發展,科學家有機會通過綜合數學和統計模型并結合組學數據來研究細胞命運的發展。
造血干細胞是研究細胞命運選擇的經典模型,在脊椎動物的骨髓里,有限的造血干細胞可以分化出體內各類成熟的血細胞,這個作用受到轉錄因子和DNA元件嚴密的平衡調控。
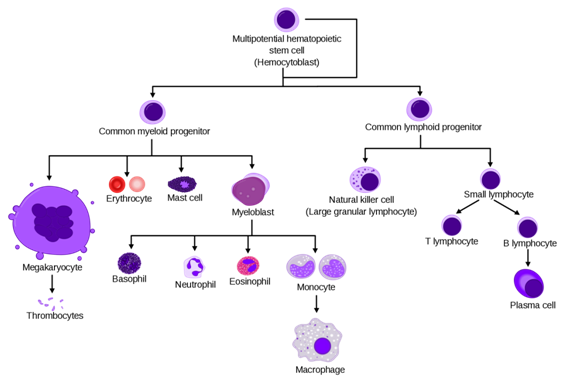
圖 | 造血干細胞分化的經典模型
(多能造血干細胞分化成髓細胞和淋巴細胞前體細胞,再進一步分化成粒細胞、紅細胞、淋巴細胞等。)(圖片來源:維基百科“造血干細胞”詞條)
盡管此前的研究通過測量RNA的表達量來量化不同子細胞中的轉錄因子的變化,但大家都知道,RNA的表達量并不等于蛋白質的表達水平。目前,來自牛津大學Weatherall研究所計算生物學中心的Morrissey博士課題組和加拿大渥太華干細胞研究中心的Brand教授課題組合作在Cell Stem Cell發表了通過單細胞蛋白質組學的方法,測定造血干細胞轉錄因子共表達譜系的時間特異性變化,首次直接提供了造血干細胞命運決定的蛋白質表達數據。

圖片來源:Cell Stem Cell 網站截圖
研究人員首先對多能干細胞(CD34+ HSPC)分化為紅細胞的完整進程(共22天,包括各個進程的紅細胞)定時取樣(每隔兩天), 在每個時間點對每個單細胞進行標記,通過27種抗體聯合標記對應的蛋白質,再通過質譜流式細胞術(CyTOF)同時測定多種蛋白質的表達,這樣科學家們就可以比較從多能造血細胞到紅細胞的分化過程中13個連續時間點的關鍵蛋白質表達水平。
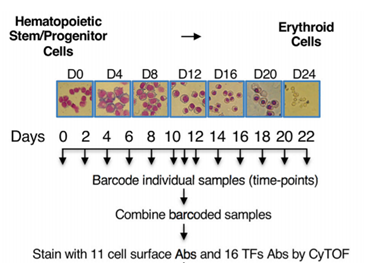
圖 | 實驗過程示意圖(圖片來源:論文)
研究人員首先使用最近鄰居算法 (KNN Algorithm)將數據可視化,通過構建蛋白質表達水平相似的細胞之間的連接網來找到不同的細胞分化路徑,發現了干細胞分化為紅細胞和巨型吞噬細胞的兩個方向的重要蛋白。為了確定具體的細胞亞型,研究人員根據CyTOF數據的統計學特性,開發了新的分類算法 (Clustering Method)—負二項分布統計法,這個算法可以根據單細胞蛋白質表達的水平進行分類,確定細胞亞型,從而比較不同細胞亞型的蛋白質水平。
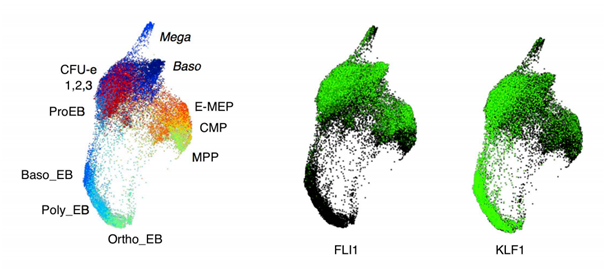
圖|FLI1和KLF1在不同細胞中的表達(圖片來源:論文)
通過開發的新算法,研究人員發現,從干細胞到紅細胞/巨型吞噬細胞的分化路徑中,轉錄因子KLF1和FLI1皆有表達,但兩者的表達水平不同,當KLF1的表達水平高于FLI1時,分化導向為紅細胞,反之,為巨型吞噬細胞,研究人員還通過實驗證實了這一分化路徑。
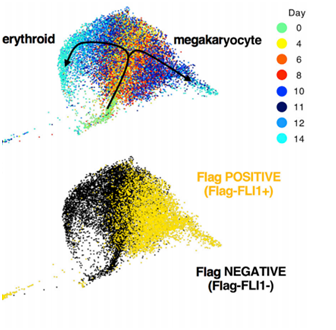
圖 | 紅細胞和巨核細胞分化路徑圖
(在某一個時間點后細胞走向了兩條完全相反的分化路徑,FLI1過表達的細胞組中,絕大部分的細胞都分化為巨型吞噬細胞。)(圖片來源:論文)
這是科學家們首次通過測量蛋白質表達水平完整地展示了造血干細胞分化過程中連續時間的轉錄因子表達水平,本研究中開發的新算法為干細胞命運決定的分析提供了新思路,該研究為更好的理解干細胞的分化的命運決定提供了數據基礎。
與此同時,該研究也為相關的血液疾病(如急性白血病)的治療提供了蛋白組學的信息,這些時空水平的蛋白質信息也對后續的藥物研發提供了理論基礎。
本文作者: 程謙博士(論文共同第一作者),先后畢業于英國牛津大學、劍橋大學,現為英國牛津大學Weatherall分子醫學研究所計算生物學中心博士后研究員,合作導師為Edward Morrissey博士,通過開發和應用數學與統計模型研究組織內的干細胞命運。
課題組主頁:https://www.imm.ox.ac.uk/research/units-and-centres/mrc-wimm-centre-for-computational-biology/groups/quantitative-biology-of-cell-fate-and-tissue-dynamics.
參考文獻:
1. Palii, C.*, Cheng, Q.*, Gillespie, M., Shannon, P., Mazurczyk, M., Napolitani, G., Price, N.D., Ranish, J.A., Morrissey, E., Higgs, D.R., Brand, M., Single-cell proteomics reveal that quantitative changes in co-expressed lineage-specific transcription factors determine cell fate. Cell Stem Cell, online
2. Palii, C.G., Pasha, R., and Brand, M. (2011). Lentiviral-mediated knockdown during ex vivo erythropoiesis of human hematopoietic stem cells. J. Vis. Exp. 2813.
3. Kester, L., and van Oudenaarden, A. (2018). Single-cell transcriptomics meets lineage tracing. Cell Stem Cell 23, 166–179.
4. Spitzer, M.H., and Nolan, G.P. (2016). Mass cytometry: single cells, many features. Cell 165, 780–791.
向左向右?它決定造血干細胞的命運
圖文簡介
多能干細胞具有分化成不同類型的子細胞的多能性。造血干細胞是研究細胞命運選擇的經典模型,在脊椎動物的骨髓里,有限的造血干細胞可以分化出體內各類成熟的血細胞,這個作用受到轉錄因子和DNA元件嚴密的平衡調控。通過開發新的算法,研究人員發現,從干細胞到紅細胞/巨型吞噬細胞的分化路徑中,轉錄因子KLF1和FLI1皆有表達,但兩者的表達水平不同,當KLF1的表達水平高于FLI1時,分化導向為紅細胞,反之,為巨型吞噬細胞.
- 來源: 科普融合創作與傳播
- 上傳時間:2019-03-15


 科普中國公眾號
科普中國公眾號
 科普中國微博
科普中國微博

 幫助
幫助