我們能否延緩衰老?這或許是每個時代、每一代人都曾提出過的問題。從煉金術士苦苦尋找長生不老藥,到當今實驗室里研發的抗老抗衰分子篩選,人類對衰老的探索從未停止。
事實上,現代社會已經大幅度延長了人均壽命。過去一個世紀,憑借醫學、營養和公共衛生的進步,越來越多的人活到了七八十歲。然而,活得更久并不總意味著活得更好。隨著年齡增長,肌肉萎縮、骨質疏松、認知減退等常規老化現象往往接踵而至,嚴重影響了晚年的生活質量。
科學界也意識到,僅僅延長壽命還不夠,健康壽命的延長,才是更具意義的目標。于是,一種被稱為Klotho蛋白的分子悄然走紅于衰老研究的舞臺。它不僅與長壽相關,還可能具有增強認知、改善肌肉和骨骼健康的能力。

基因治療使小鼠健康的長壽示意圖(圖片來源:作者使用AI生成)
那么,這種蛋白質真的能讓身體年輕嗎?一項剛剛發表的新研究通過基因治療手段,在小鼠體內提升Klotho蛋白的水平,結果不僅延長了壽命,還顯著改善了身體和大腦的功能。研究團隊認為,這一成果為未來人類抗衰老治療提供了全新的可能。
Klotho蛋白到底是什么?它有什么“抗老”本事?
Klotho,這個名字源于希臘神話中掌管生命絲線的命運三女神之一——克羅托(Clotho)。她象征著生命的開端,而Klotho蛋白,在生物學領域中似乎也確實與延長生命息息相關。
Klotho蛋白最早在1997年被發現于小鼠體內,當研究人員敲除該基因后,實驗鼠迅速出現多種衰老相關癥狀,如骨質疏松、皮膚變薄、認知障礙等,壽命大幅縮短。而當研究人員過度表達Klotho時,壽命又顯著延長。這一現象立即引發了科學界對Klotho功能的極大興趣。
Klotho蛋白有三種主要形式,一種是膜結合型(m-KL),是最初由基因轉錄產生的全長蛋白,嵌于細胞膜上,尤其在腎臟和腦組織中較多。另一種是可溶型(p-KL),由膜型蛋白經酶切后釋放入血液,可在全身發揮調節作用,還有一種是分泌型(s-KL),由另一種剪接形式產生,直接以可溶狀態分泌入體液,擁有獨立的C端結構,不依賴于酶剪切。
在功能層面,Klotho蛋白可謂是“抗老多面手”。在調節關鍵信號通路方面,它可影響胰島素、胰島素樣生長因子-1等信號通路,這些都是與衰老、代謝和細胞增殖密切相關的核心機制。在抗氧化、抗炎反應反面,Klotho能夠減少自由基產生、降低慢性炎癥水平,緩解與年齡相關的細胞損傷。還能影響鈣磷代謝,通過與成纖維生長因子23協同作用,調控腎臟對磷的重吸收,有助于維持骨骼穩態。除此之外,研究還發現,Klotho有助于維持神經元的結構與功能,促進神經再生,還能減輕阿爾茨海默癥小鼠模型中的病理損傷。
相比于p-KL,s-KL更安全,不干擾礦物質代謝,更適合用作治療手段。因此,在本次研究中,科學家們選擇將s-KL作為“藥物候選分子”,進行系統性測試,觀察它在延緩衰老方面的真實效力。
“返老還童”的證據:s-KL在小鼠身上的驚人效果
為了驗證s-KL是否真的能延緩衰老、提升健康狀態,研究團隊設計了一項嚴謹的動物實驗。他們采用一種常用于人類基因治療研究的工具——AAV9病毒載體,將s-KL基因導入健康小鼠體內,并通過靜脈注射和腦室注射的方式,實現全身和大腦同時高表達s-KL。處理分為兩個時間點:一組在6月齡時接受治療(相當于20-25歲的人類),另一組在12月齡時接受治療(相當于38-47歲的人類),均持續觀察至24月齡,約等于人類70歲。
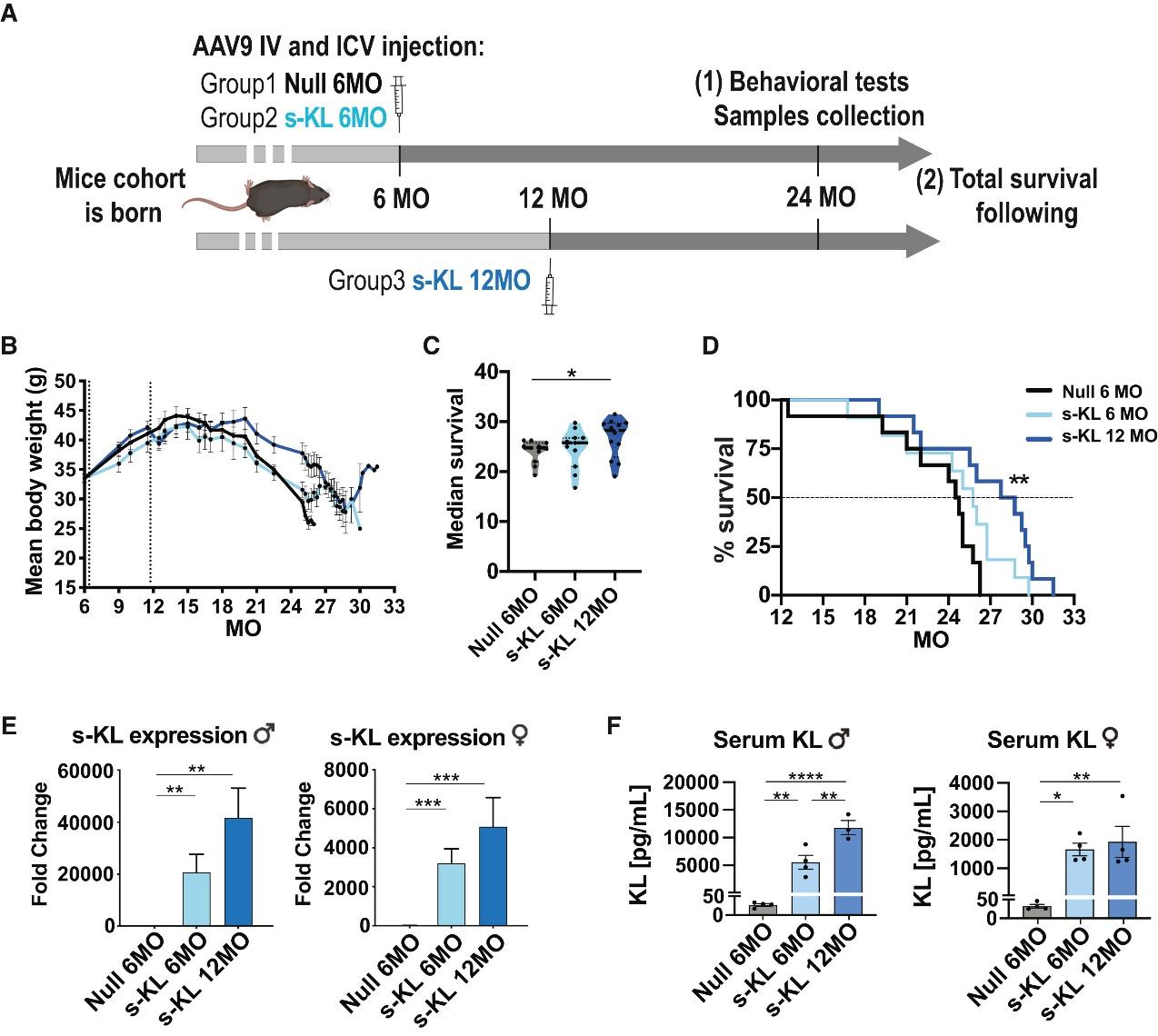
定期接受治療的小鼠(圖片來源:參考文獻[1])
結果令人驚訝,小鼠的壽命顯著延長。其中,12月齡注射s-KL的小鼠群體壽命延長了近20%,中位生存期從24.6個月提高到28.3個月。這是首次在野生型非病態小鼠中,通過一次性基因介入治療實現如此明確的延壽效果。
更重要的是,s-KL并非只是讓小鼠“活得更久”,而是“活得更健康”。首先體現在肌肉功能的提升上。在一系列行為測試中,接受s-KL治療的小鼠在懸桿、轉棒和握力測試中的表現明顯優于對照組,尤其是12月齡開始干預的個體,成績更加突出。組織學觀察顯示,這些小鼠的肌肉纖維直徑增大,結構更為緊致,且肌肉中的纖維化程度顯著減輕。在肌肉移植實驗中,s-KL處理組肌肉的再生能力也表現出優勢,不僅有更多的肌源性干細胞(PAX7陽性)出現,而且增殖活躍的標志物Ki67與肌肉分化相關的MyoD表達均明顯上升,說明其具備促進肌肉修復和再生的潛力。
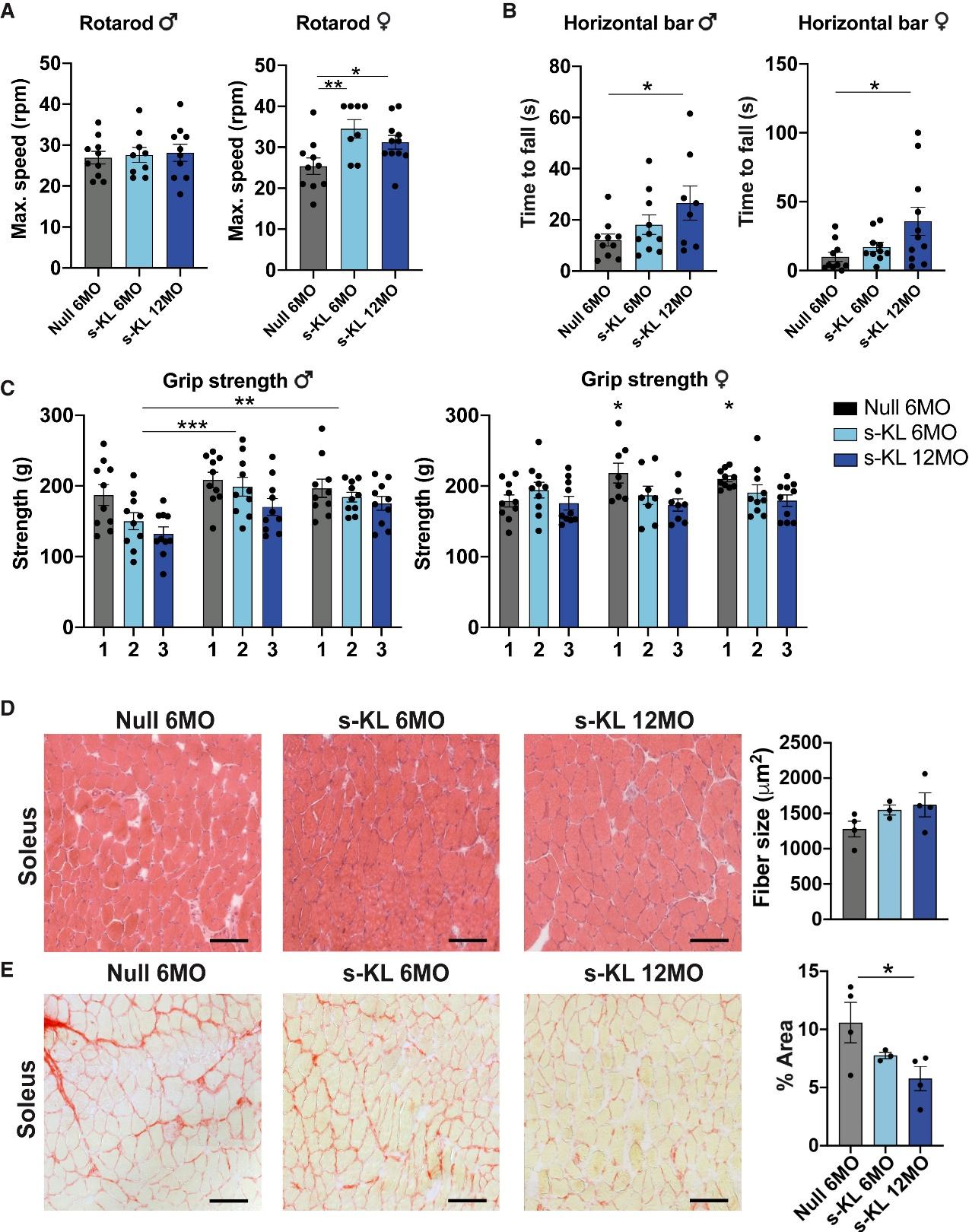
接受治療小鼠肌肉纖維對照圖片(圖片來源:參考文獻[1])
其次,s-KL對于骨骼結構也有積極影響。微型CT掃描結果顯示,雌性小鼠在接受s-KL治療后,其骨小梁數量增多、厚度增加、間隙變小,骨架整體更為緊密。與此相符的是,一些與骨形成相關的基因如Runx2、Bglap和Col1a1的表達也被顯著上調,提示s-KL可能通過調節骨代謝,發揮對骨質疏松的潛在預防作用。
在神經系統層面,s-KL也表現出保護效應。接受治療的老年小鼠其海馬區神經干細胞數量增加,未成熟神經元數量上升,且顆粒細胞層厚度也有提升,說明神經新生得到了部分恢復。同時,免疫組化結果表明,其腦部膠質細胞標志物如Iba1和GFAP表達水平上升,表明清除神經損傷的吞噬活性增強。而炎癥因子IL-12水平下降、抗炎因子IL-10升高,說明s-KL不僅激活了免疫系統,也幫助維持了中樞神經系統的免疫穩態。
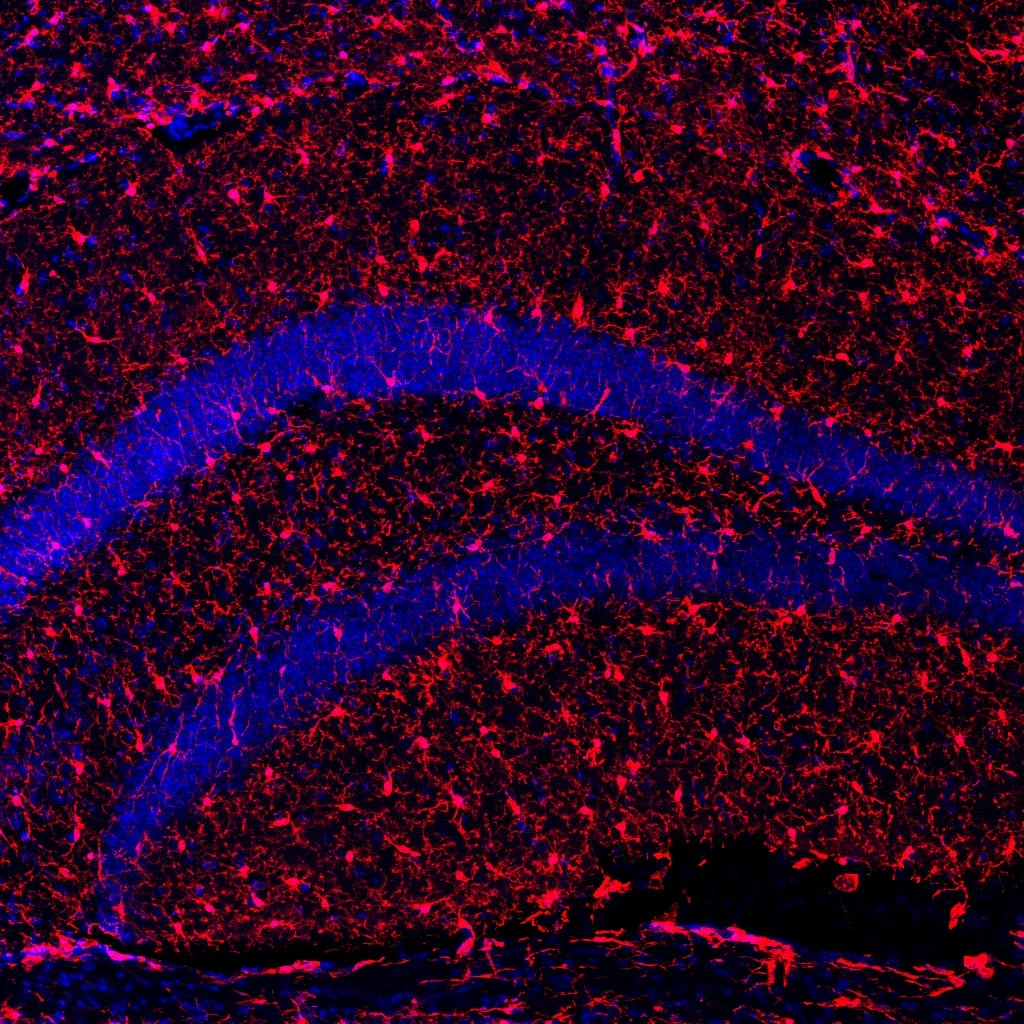
接受s-KL治療的小鼠海馬體小膠質細胞(大腦免疫系統的一部分,紅色部分)的顯微鏡圖像(圖片來源:參考文獻[1])
從分子層面來看,RNA測序分析進一步揭示了s-KL治療的深層機制。與對照組相比,s-KL處理組老年小鼠的基因表達譜更接近年輕小鼠,特別是在能量代謝、抗氧化與神經炎癥等通路上呈現出更年輕的特征。值得注意的是,神經修復、吞噬活性和免疫調節等相關基因表達被激活,而與線粒體功能障礙和慢性炎癥相關的基因表達受到抑制,說明s-KL可能從根本上重塑了老年大腦的功能狀態。簡而言之,這項研究不僅證明了s-KL具有多器官的抗衰老能力,還為“系統性干預衰老過程”提供了一個全新角度,只要提升一種內源蛋白,就可能同步改善肌肉、骨骼、大腦三大系統,真正實現“延壽又延健”。
總結
科學家常說,衰老不是一種疾病,卻是萬病之源。而這項研究告訴我們,有些源頭也許真的可以被調整。通過提升一種名叫Klotho的蛋白水平,小鼠不僅活得更久,還跑得更快、骨頭更硬、腦子也更靈光。這不是科幻小說里的青春逆轉,而是科學家一步一步用實驗數據搭建的抗衰老拼圖。雖然人類距離臨床應用還有不少障礙,但我們至少知道了——延緩衰老,可能不再只是幻想。
參考文獻:
[1] Roig-Soriano, Joan, et al. "Long-term effects of s-KL treatment in wild-type mice: Enhancing longevity, physical well-being, and neurological resilience." Molecular Therapy 33.4 (2025): 1449-1465.
[2]Kuro-o, M.. Klotho. Pflügers Archiv-European Journal of Physiology, 459.2 (2010): 333-343.
[3] Wang, Y., & Sun, Z.. Current understanding of klotho. Ageing research reviews, 8.1 (2009): 43-51.
[4] Xu, Y., & Sun, Z.. Molecular basis of Klotho: from gene to function in aging. Endocrine reviews, 36.2 (2015): 174-193.
[5] Kurosu, H., Yamamoto, M., Clark, J. D., Pastor, J. V., Nandi, A., Gurnani, P., ... & Kuro-o, M.. Suppression of aging in mice by the hormone Klotho. Science, 309.5742 (2005),:1829-1833.
作者丨Denovo科普團隊(褚宏偉博士 湖南師范大學碩士生導師;楊超博士)
審核丨趙寶鋒博士 遼寧生命科學學會
來源: 科普中國創作培育計劃
內容資源由項目單位提供


 科普中國公眾號
科普中國公眾號
 科普中國微博
科普中國微博

 幫助
幫助
 科普中國創作培育計劃
科普中國創作培育計劃 
