在紐約洛克菲勒大學的一間實驗室里,科學家們做了這樣一個大膽的實驗,他們將一種名為 NOVA1 的人類語言相關基因的變體導入小鼠體內。這個變體其實只涉及一個氨基酸分子改動——第197位氨基酸由異亮氨酸換成了纈氨酸,但它是現代人類與尼安德特人之間的重要遺傳差異之一。研究團隊好奇,這個在人類語言進化中被自然選擇留下的“微小突變”,究竟是否藏著我們語言能力的某種秘密。
結果讓人驚訝。帶有這個人類版本基因的小鼠,從小的叫聲就變得不同,音調更高,節奏也更復雜。等它們長大后,雄性在追求配偶時甚至“唱”出了比普通小鼠更復雜的情歌。
它們并沒有突然獲得語言能力,但顯然,它們說話的方式已經變了。這是一種接近語言邊界的嘗試——用遺傳學手段,去觸碰人類最獨特的能力之一:說話。
NOVA1:一種“語言感”的遺傳密碼
在復雜的人類語言背后,是否存在某種基因編碼?科學家長期試圖解答這個問題。人類之所以能夠進行抽象思維、使用語法、表達情緒,很大程度上依賴于大腦中復雜的神經回路與精密的調控機制。而這背后,正是基因在悄悄指揮一切。
在眾多語言候選基因中,一個名叫 NOVA1 的基因引起了科學家的高度關注。它是一種 RNA 結合蛋白,主要在中樞神經系統中表達,參與調控神經元中的基因剪輯過程——即可變剪接。簡單來說,它像一位“編輯師”,決定哪些基因片段被拼接進最終的蛋白產物中,從而影響神經元的功能與連接模式。
特別有意思的是,NOVA1 的第197個氨基酸位點,在現代人類與尼安德特人之間存在一個關鍵差異,我們是纈氨酸(Valine, V),他們是異亮氨酸(Isoleucine, I)。別小看這僅僅一個氨基酸的變化——在超高保守的 NOVA1 蛋白中,它位于核心結構域(KH2)內,是 RNA 識別和結合的關鍵區域。而且,這個變體在全球人類群體中幾乎固定存在,提示它可能在遠古時期經歷了強烈的自然選擇壓力。
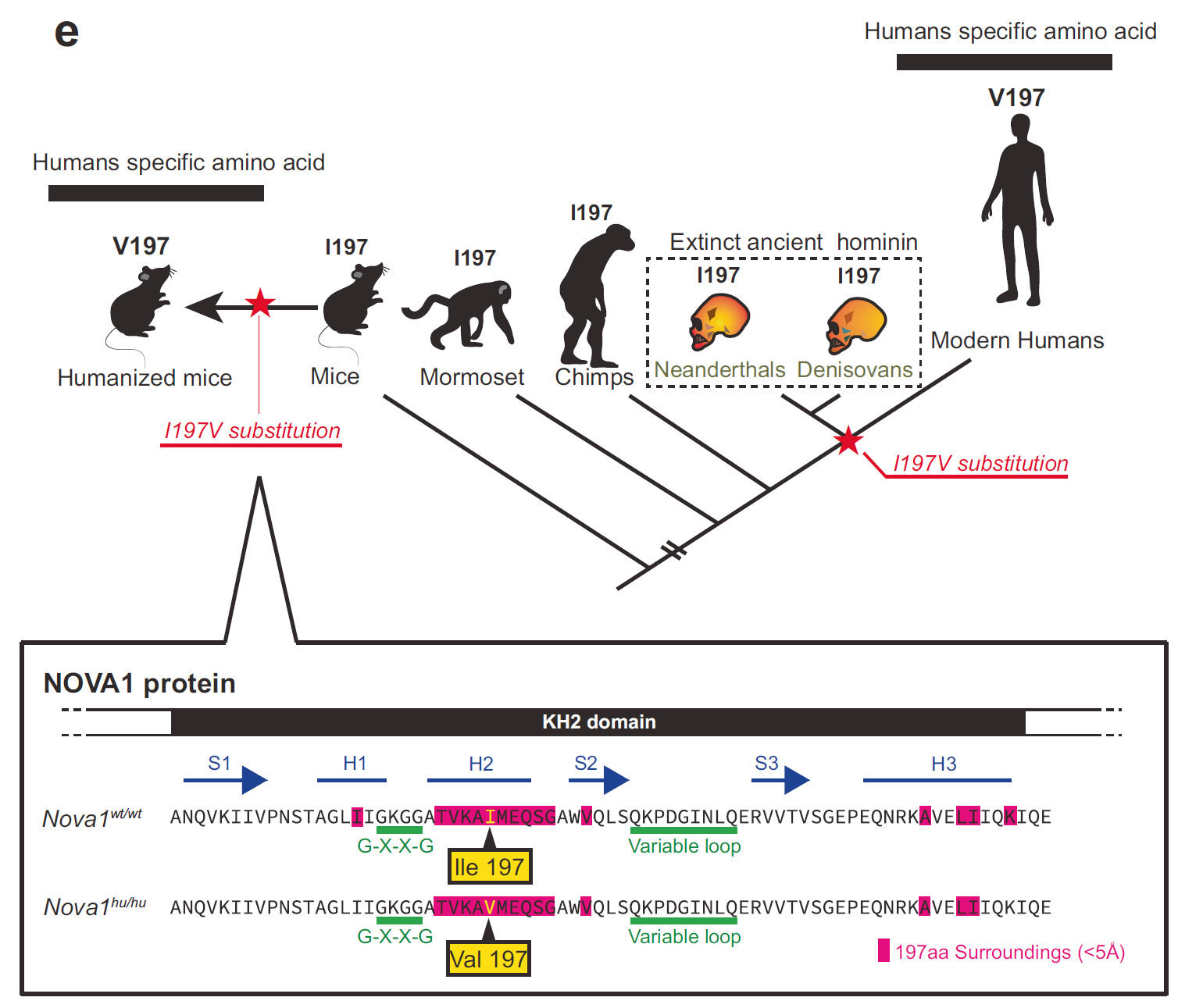
NOVA1基因第197個氨基酸變化的進化時間模型(圖片來源:參考文獻[1])
進化基因組學分析表明,這種 NOVA1 的人類特有版本(I197V)可能出現在20萬年前非洲的某一支現代智人祖先中,后來隨這群人類擴散到全世界,成為現代人共同的遺傳特征之一。而尼安德特人、丹尼索瓦人等表親們則沒有這種突變。這一細節令人浮想聯翩——難道是這個微小的分子差異,讓我們的祖先在語言能力上邁出了一步?
值得一提的是,NOVA1 不只是一個語言相關的遺傳因素,它還與神經發育疾病有關。一些攜帶 NOVA1 缺失突變的人類患者,往往表現出語言遲緩、多動和社交障礙等癥狀。而在小鼠中,刪除 NOVA1 基因則會導致出生后因運動功能異常快速死亡,說明它對神經系統功能至關重要。
不過,光有這些線索還遠遠不夠。為了驗證 NOVA1 的這個微小突變是否真的影響語言相關的功能,科學家們決定做一件更直接的事,把它移植進老鼠體內,然后看看會發生什么。
老鼠也能“說得更復雜”?
在這項研究中,科學家利用基因編輯技術將人類特有的 NOVA1 變體(I197V)引入小鼠體內,生成了“人源化”小鼠。這些小鼠在生長發育和腦結構上與普通小鼠無異,但當它們開口說話時,卻展現出了明顯不同的特征。
研究團隊發現,剛出生幾天的“人源化”小鼠在與母鼠分離時發出的超聲波叫聲與普通小鼠相比,在頻率、音調結構和節奏上都更為復雜。它們發出的音節不僅音調更高,且常帶有更多變化,例如音高跳躍和多重音段。這類變化雖然我們肉眼難察,但通過聲音頻譜圖分析,可清晰看出其“語言結構”更為豐富。
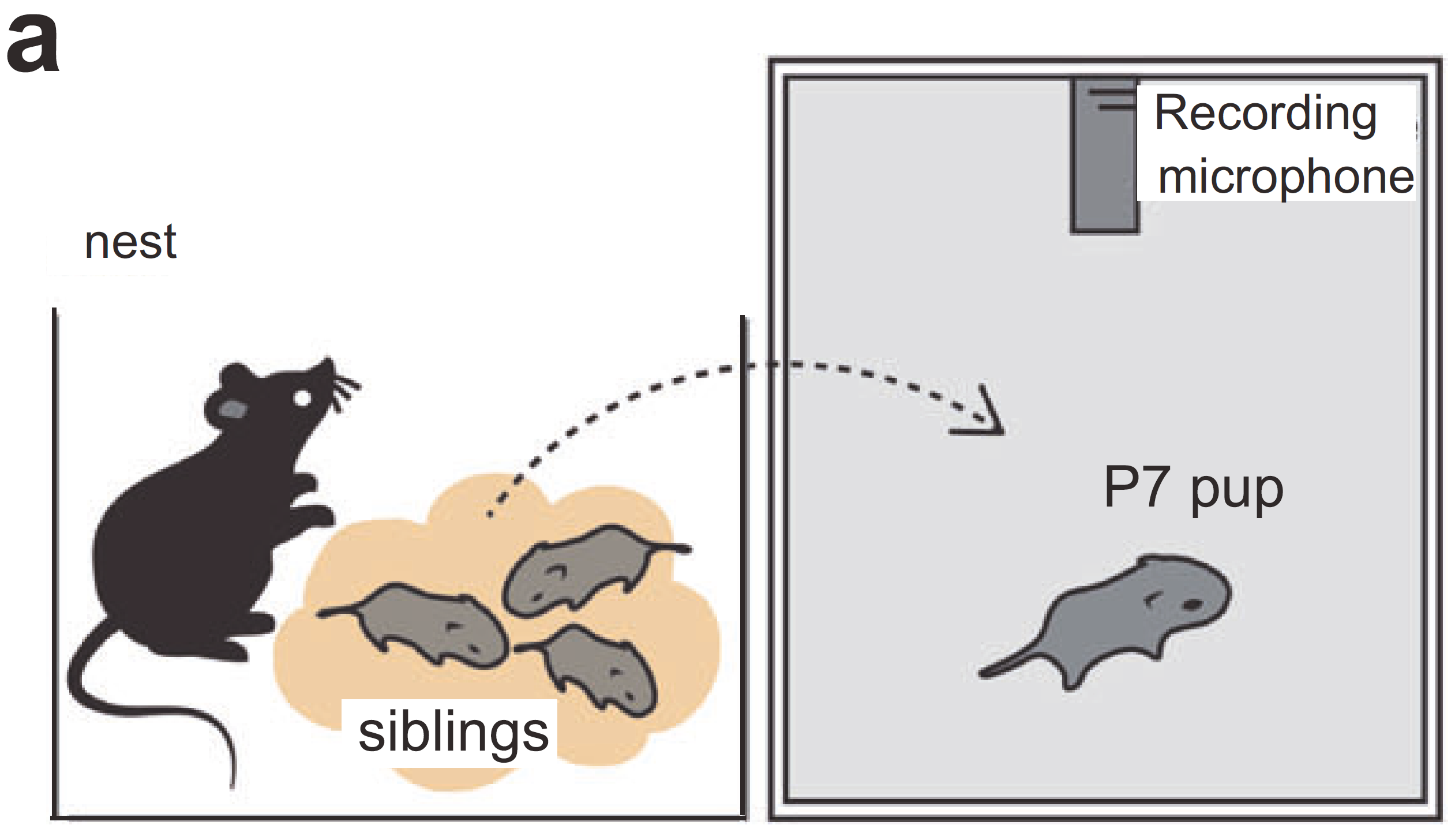
幼崽的隔離誘導超聲波發聲 (USV) 測試(圖片來源:參考文獻[1])
成年雄鼠的表現更加明顯。在求偶實驗中,這種小鼠發出的叫聲擁有更高的最大頻率、更多跳躍音調和更復雜的節奏。這些被認為是老鼠情歌的信號,在自然環境中可能增強其吸引配偶的能力。盡管母鼠在行為測試中對這些聲音沒有表現出顯著偏好,但聲音本身的變化已經證明,僅一個氨基酸的改變,就足以調控發聲模式的精細差異。
從分子機制看,研究表明這些發聲差異與大腦中特定區域的基因剪接變化有關,尤其集中在中腦導水管周圍灰質等控制先天發聲的神經區域。研究還發現,多個與發聲行為密切相關的基因在這些“人源化”小鼠中發生了剪接變異,其中包括已知與語言障礙、神經發育和自閉癥相關的基因如 Auts2 和 Nrxn2。這些發現提示我們,語言能力的演化或許正是通過一系列微妙但關鍵的分子調控,逐步塑造出更復雜的表達潛能。
總結
人類語言的起源,或許遠比我們想象的復雜,也更微妙。它不是單一基因的產物,而是千百個調控因子的協同結果。但這項研究提醒我們,有些看似微不足道的遺傳變異,可能正是那個轉折點——讓我們從簡單的叫喊走向復雜的表達。語言不是一蹴而就的奇跡,而是一場緩慢而堅定的進化。
參考文獻:
[1] Tajima Y, Vargas C D M, Ito K, et al. A humanized NOVA1 splicing factor alters mouse vocal communications[J]. Nature Communications, 16.1 (2025): 1542.
[2] Chabout, Jonathan, et al. "A Foxp2 mutation implicated in human speech deficits alters sequencing of ultrasonic vocalizations in adult male mice." Frontiers in behavioral neuroscience 10 (2016): 197.
[3] Meyer, Matthias, et al. "A high-coverage genome sequence from an archaic Denisovan individual." Science 338.6104 (2012): 222-226.
[4]Jarvis, Erich D. "Evolution of vocal learning and spoken language." Science 366.6461 (2019): 50-54. [5]
作者丨邵文亞博士 福建醫科大學副教授;楊超 博士
審核丨趙寶鋒博士 遼寧生命科學學會
來源: 科普中國創作培育計劃
內容資源由項目單位提供


 科普中國公眾號
科普中國公眾號
 科普中國微博
科普中國微博

 幫助
幫助
 科普中國創作培育計劃
科普中國創作培育計劃 
