一氧化氮(NO)曾普遍被視為一種有毒有害氣體,應(yīng)盡可能遠離。然而,后來的科學(xué)研究揭示它在生物體內(nèi)發(fā)揮極為重要的生理作用,NO是首個被發(fā)現(xiàn)在動物體內(nèi)起到氣體信號分子作用的物質(zhì)。這項開創(chuàng)性的工作是由美國藥理學(xué)家斐里德·穆拉德通過實驗闡明的,最初他意外發(fā)現(xiàn)了含氮物質(zhì)能夠激活特定的酶,進而揭開了硝酸甘油治療心絞痛的機理——即一氧化氮分子介導(dǎo)的信號轉(zhuǎn)導(dǎo)能夠促使平滑肌舒張;同時進一步證實了內(nèi)源性NO的存在。本文將主要介紹穆拉德的科研歷程,展示他如何逐步取得這項重大發(fā)現(xiàn),見證科學(xué)與生命的奇妙邂逅。
撰文 | 郭曉強(河北體育學(xué)院)
提到一氧化氮(Nitric oxide,NO),大家第一印象是一種有毒氣體和環(huán)境污染物,事實也的確如此,但這種看法忽視了它在人體中的重要作用。
NO無色無味,于1779年由英國著名化學(xué)家約瑟夫·普利斯特里(Joseph Priestley)首先發(fā)現(xiàn),他還發(fā)現(xiàn)一氧化二氮、二氧化氮、氧氣、氨氣、氯化氫等眾多氣體。后續(xù)研究中,NO都被看作大氣污染物,是煙草、柴油和汽油等燃燒副產(chǎn)品,經(jīng)機動車排放、工業(yè)排放和微生物釋放等過程產(chǎn)生。毒理學(xué)實驗顯示,吸入一定量NO(具體數(shù)值可能因條件和個體差異而異)可導(dǎo)致輕度呼吸急促和咳嗽,一段時間后出現(xiàn)支氣管痙攣和肺水腫;吸入高濃度NO會造成燒傷、痙攣、喉嚨組織腫脹、上呼吸道阻塞甚至死亡。工作場所NO濃度允許上限為8小時內(nèi)25ppm(part per million,百萬分之一),當(dāng)達到100ppm時對生命和健康造成嚴(yán)重危險。
直到20世紀(jì)70年代,美國藥理學(xué)家斐里德·穆拉德(Ferid Murad)首先揭示了其有益的一面,并進一步發(fā)現(xiàn)它在體內(nèi)還發(fā)揮著至關(guān)重要的生理功能,NO這個“百害而無一利”的標(biāo)簽才被去除。穆拉德也因此與他人共享了1998年的諾貝爾生理學(xué)或醫(yī)學(xué)獎。

斐里德·穆拉德(Ferid Murad,1936.9.14—2023.9.4)
一
志存高遠
1936年9月14日,穆拉德出生于美國印第安納州懷廷市一個移民家庭。父親來自阿爾巴尼亞,以經(jīng)營小雜貨店為生,因此經(jīng)濟條件有限,全家五口擠在一個不滿50平米的小房間。父母辛苦勞作維持生計,每日工作很長時間,這為穆拉德帶來很大影響,他從小就下定決心努力學(xué)習(xí),以不再像父母這樣辛勞。穆拉德在12歲時就樹立成為一名醫(yī)生的理想,但“事與愿違”的是,穆拉德后來的工作比父母時間更長且更努力,區(qū)別在于不再是僅僅為了生計。
高中畢業(yè)后,穆拉德面臨一大抉擇。由于家庭難以承擔(dān)高額學(xué)費,因此他需要尋找一所能夠提供高額獎學(xué)金的大學(xué)。穆拉德最初決定考取免費的海軍學(xué)院或西點軍校,但這些學(xué)校不講授醫(yī)學(xué)課程,畢業(yè)后的四年兵役會耽擱醫(yī)學(xué)深造。他最終選擇迪堡大學(xué)(DePauw University)。迪堡大學(xué)是一所小型而優(yōu)秀的文理大學(xué),學(xué)校為穆拉德提供一份獎學(xué)金保障其完成學(xué)業(yè),這里開設(shè)生物學(xué)和化學(xué)等醫(yī)學(xué)相關(guān)課程,為他進一步醫(yī)學(xué)深造提供了便利。
1957年,大四的穆拉德準(zhǔn)備申請醫(yī)學(xué)院,最初決定去位于圣路易斯的華盛頓大學(xué)醫(yī)學(xué)院,隨后兩個人的建議讓他徹底改變了主意。一位是穆拉德大學(xué)期間選修科研時的導(dǎo)師福斯特·富勒(Forst Fuller),建議他考慮西儲大學(xué)(Case Western Reserve University)新開設(shè)的基礎(chǔ)和臨床聯(lián)合七年制醫(yī)學(xué)博士課程;另一位是摯友比爾·薩瑟蘭(Bill Sutherland)的父親厄爾·薩瑟蘭(Earl Wilbur Sutherland),他是該課程的發(fā)起人和負(fù)責(zé)人,為穆拉德更詳細(xì)地介紹了課程優(yōu)點,包括免除學(xué)費外加每月2000美元津貼,誘人條件使穆拉德最終選擇西儲大學(xué)。
二
師出無名
在穆拉德進入西儲大學(xué)前,厄爾·薩瑟蘭已取得一項重大發(fā)現(xiàn)。1957年,薩瑟蘭和助手西奧多·拉爾(Theodore Rall)研究腎上腺素促進糖原分解機制時發(fā)現(xiàn),把腎上腺素添加到完整肝勻漿可促進糖原分解;然后將肝勻漿離心分離成上清液(細(xì)胞質(zhì)部分)和沉淀(細(xì)胞膜部分)兩部分后,僅將腎上腺素再次加入上清液中,未發(fā)現(xiàn)肝糖原分解明顯增加,但重新加入沉淀后,糖原分解活性恢復(fù),這一結(jié)果表明細(xì)胞膜是腎上腺素發(fā)揮生理活性所必備的。他們進一步使用腎上腺素處理細(xì)胞膜沉淀,同時補充能量分子ATP后生成一種耐熱小分子物質(zhì),將該物質(zhì)直接加入(不使用腎上腺素)上清部分也可增加糖原分解,最終確定該物質(zhì)為環(huán)腺苷酸(cyclic adenosine 3'5'-monophosphate,cAMP)。薩瑟蘭在此發(fā)現(xiàn)基礎(chǔ)上提出著名的“第二信使假說”,即激素作用于細(xì)胞膜特定受體并激活腺苷酸環(huán)化酶(adenylate cyclase,AC)生成cAMP,cAMP進一步發(fā)揮活性實現(xiàn)生理效應(yīng);在這里激素是第一信使,cAMP為第二信使。薩瑟蘭因這一貢獻獲得1971年諾貝爾生理學(xué)或醫(yī)學(xué)獎。
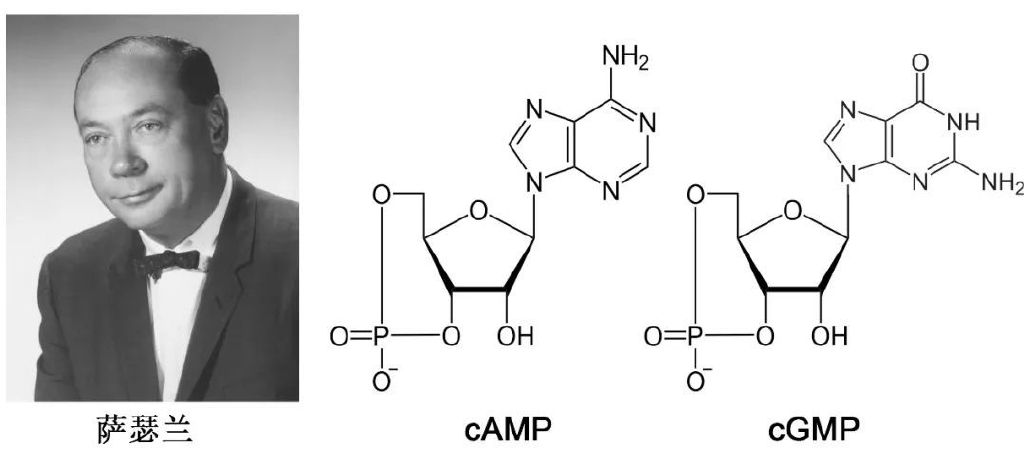
薩瑟蘭的重大發(fā)現(xiàn)
薩瑟蘭和拉爾聯(lián)合指導(dǎo)穆拉德從事cAMP研究。穆拉德任務(wù)是探索兒茶酚胺對cAMP形成的影響。在此過程中,他發(fā)現(xiàn)乙酰膽堿可抑制腺苷酸環(huán)化酶,從而減少cAMP生成,這是首次描述激素對cAMP的負(fù)調(diào)控,第二信使假說內(nèi)容更為豐富了。當(dāng)時,第二信使假說領(lǐng)域快速發(fā)展,穆拉德作為見證者幾乎每天能看到新進展和新發(fā)現(xiàn);他也是參與者,并激發(fā)出巨大科研興趣,最終放棄了原本的醫(yī)生夢。另一方面,從這些研究中,他熟練掌握了cAMP及其他相似化合物的檢測方法,為將來科研打下了良好基礎(chǔ)。
1963年,薩瑟蘭在尿液中發(fā)現(xiàn)一種和cAMP結(jié)構(gòu)高度相似的小分子cGMP(環(huán)鳥苷酸),隨后發(fā)現(xiàn)其廣泛存在。薩瑟蘭最初推測二者同樣重要,但事實并非如此:用作研究的激素都通過cAMP介導(dǎo)反應(yīng),均不依賴cGMP,這便留下一個重要的未解之謎——cGMP的功能是什么?這一問題成為穆拉德將來的科研方向。
1965年,穆拉德獲得博士學(xué)位后進入麻省總醫(yī)院完成2年的實習(xí)工作,隨后加入國立健康研究院從事三年多博士后工作。1970年,弗吉尼亞大學(xué)醫(yī)學(xué)系新建一個臨床藥理部門,穆拉德加入并組建自己的科研小團隊,開啟獨立研究。
三
平淡無奇
選擇一個合適研究方向是穆拉德首先需要解決的問題,當(dāng)時可選cAMP和cGMP兩種分子,二者雖然結(jié)構(gòu)極為相似,境遇卻大相徑庭——一個大紅大紫、一個默默無聞;一個風(fēng)光正盛、一個少人問津。穆拉德不想隨波逐流,他秉持“天生我才”理念,既然細(xì)胞可產(chǎn)生cGMP,那cGMP就應(yīng)有獨特作用,只是目前尚未發(fā)現(xiàn)而已。
當(dāng)時已知細(xì)胞有兩類催化cGMP生成的鳥苷酸環(huán)化酶(GC),一類位于細(xì)胞膜,另一類位于細(xì)胞質(zhì)。穆拉德選擇位于細(xì)胞質(zhì)的GC,實驗設(shè)計較為簡單,他將細(xì)胞進行破碎,離心去掉沉淀保留上清,然后觀察不同物質(zhì)對鳥苷酸環(huán)化酶活性的影響,方法是檢測cGMP生成量(穆拉德已熟練掌握)。穆拉德短期內(nèi)也不準(zhǔn)備對酶進行純化(較為耗時),因此使用粗制品進行研究,但需要將大量制備出的剩余樣品及時儲存。當(dāng)時實驗室最常用的蛋白保存試劑為疊氮化鈉,對保存后的樣品進行檢測時,穆拉德意外發(fā)現(xiàn)鳥苷酸環(huán)化酶活性大幅度增加,cGMP生成量顯著升高。這一意外發(fā)現(xiàn)使穆拉德十分驚訝,就把實驗室可用的試劑依次進行測試,結(jié)果發(fā)現(xiàn)多種化合物如羥胺、苯肼和亞硝酸鹽等也顯著激活酶活性,它們擁有一個共同特征,那就是都含氮元素,深入分析發(fā)現(xiàn)它們激活鳥苷酸環(huán)化酶原因在于反應(yīng)中生成了NO。
穆拉德還發(fā)現(xiàn),這些物質(zhì)不僅增加粗制品鳥苷酸環(huán)化酶活性,而且對完整細(xì)胞也具有活性。當(dāng)使用這些化合物處理平滑肌細(xì)胞,可明顯增加細(xì)胞內(nèi)cGMP含量;重要的是,能進一步引起肌細(xì)胞舒張,而這是血管擴張的基本原理。因此,穆拉德決定進一步測試有實用價值的化合物,這些化合物要含氮并具有血管舒張活性,在此標(biāo)準(zhǔn)下他鎖定治療心絞痛的藥物——硝酸甘油。
四
意外之喜
1847年,意大利化學(xué)家阿斯卡尼奧·索布雷洛(Ascanio Sobrero)首次在實驗室制備出硝酸甘油(許多人都錯誤認(rèn)為硝酸甘油由諾貝爾首先發(fā)現(xiàn)),這是一種揮發(fā)性極強且極易爆炸的液體(索布雷洛本人實驗過程中傷痕累累);19世紀(jì)60年代,諾貝爾將硝酸甘油進行改進研制出固態(tài)炸藥。令人意想不到的是,不久人們發(fā)現(xiàn)硝酸甘油可用于治療心絞痛,后續(xù)又成功開發(fā)出單硝酸異山梨醇酯、硝普鈉等多種藥物,統(tǒng)稱硝酸鹽血管舒張劑,但藥理一直不詳。
1977年,穆拉德測試硝酸甘油,發(fā)現(xiàn)可增加血管平滑肌cGMP含量并引起肌肉松弛,原因在于它也可產(chǎn)生NO。這項研究有效解釋了硝酸甘油等藥物治療心絞痛的藥理機制,那就是生成NO生成后,由NO提升cGMP含量,從而實現(xiàn)平滑肌舒張。這一發(fā)現(xiàn)直接為新藥研發(fā)指明方向。1986年,輝瑞公司設(shè)立研發(fā)小組篩選治療心絞痛新藥,原理是尋找磷脂酶5(該酶降解cGMP)抑制劑,最終得到西地那非。該藥可有效增加cGMP濃度,具有擴張冠狀動脈和抑制血栓形成的作用。隨后臨床試驗卻發(fā)現(xiàn)西地那非對心絞痛緩解作用非常有限,而意外觀察到對男性勃起功能障礙有奇效,這一偶然發(fā)現(xiàn)促使神藥“偉哥”誕生,穆拉德也因此獲得“偉哥之父”的美譽。
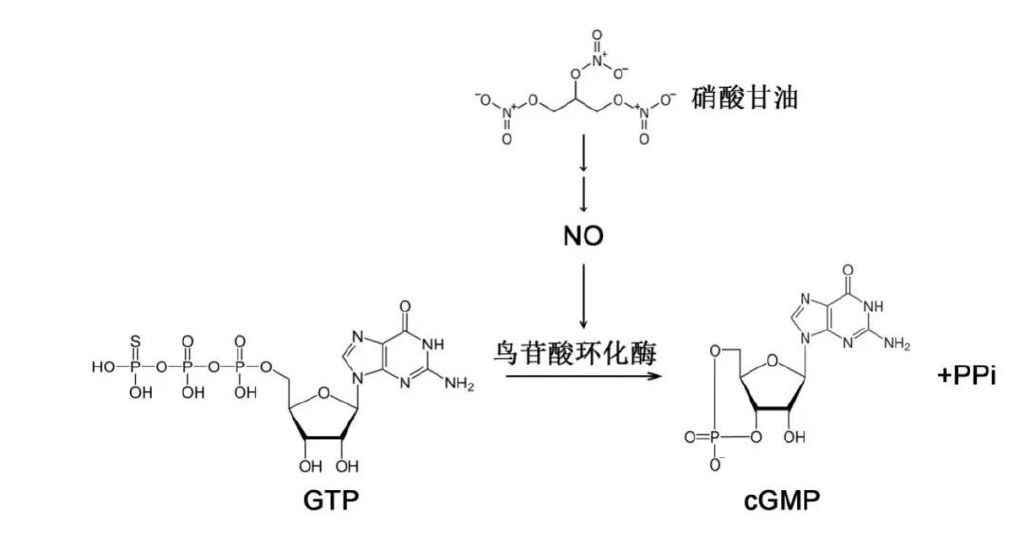
硝酸甘油、NO和cGMP
穆拉德的思想并未簡單停留在硝酸甘油藥理機制,而是進一步提出存在內(nèi)源性NO,即正常細(xì)胞可在激素和神經(jīng)遞質(zhì)等刺激下由自身含氮化合物產(chǎn)生NO,進而通過誘導(dǎo)cGMP生成發(fā)揮生理作用。按照推測,內(nèi)源性NO含量既低,存在時間又短(這一特性避免其毒性發(fā)揮)。當(dāng)時最先進技術(shù)都很難直接檢測NO,一些證據(jù)間接證實內(nèi)源NO存在,但并不太令人信服,因此遲遲未獲科學(xué)界普遍接受,直到另一個偶然發(fā)現(xiàn)。
五
最佳助攻
20世紀(jì)50年代,紐約州立大學(xué)藥理學(xué)家羅伯特·弗奇戈特(Robert Furchgott)研究血管擴張的原因,關(guān)注點是神經(jīng)遞質(zhì)乙酰膽堿。將乙酰膽堿注射到動物體內(nèi)可引起血管擴張和血壓下降現(xiàn)象,因此他推測乙酰膽堿可引起血管中肌細(xì)胞舒張,從而增加血管直徑。弗奇戈特讓學(xué)生用體外實驗驗證這一推測,他們制備出一系列血管條,然后使用乙酰膽堿處理;如果血管條變長則意味著肌細(xì)胞舒張,奇怪的是結(jié)果重復(fù)性極差,更多情況下出現(xiàn)血管條變短現(xiàn)象,和預(yù)期完全相反,對這一現(xiàn)象一直無法解釋。
1978年,弗奇戈特決定重新研究這個問題,這次實驗者選擇使用血管環(huán),結(jié)果發(fā)現(xiàn)乙酰膽堿處理造成血管擴張,而且結(jié)果非常穩(wěn)定。進一步分析發(fā)現(xiàn),兩次實驗的差別就在使用的材料上,血管環(huán)不影響血管內(nèi)部的內(nèi)皮細(xì)胞,而血管條制備過程通常會破壞內(nèi)皮細(xì)胞。對此,他們將血管環(huán)內(nèi)部也去掉內(nèi)皮細(xì)胞,結(jié)果用乙酰膽堿處理后,血管也不再擴張;制備保留內(nèi)皮細(xì)胞的血管條用乙酰膽堿處理后則血管舒張,與之前的結(jié)果一致;甚至他們制備出三明治結(jié)構(gòu),那就是一條血管保留內(nèi)皮,另一條去除,然后放置于一起(內(nèi)皮細(xì)胞居中),用乙酰膽堿處理可造成兩條血管均舒張。這一系列結(jié)果表明乙酰膽堿作用于肌細(xì)胞需內(nèi)皮細(xì)胞生成一種特定中介物,弗奇戈特將其稱為內(nèi)皮來源舒張因子(EDRF)。弗奇戈特?zé)o法分離和確定EDRF是何種物質(zhì),但它的功能引起穆拉德的巨大興趣,因此與弗奇戈特溝通準(zhǔn)備合作研究,但由于其他原因而被耽擱。
六
殊途同歸
EDRF的發(fā)現(xiàn)引起許多研究人員巨大興趣,世界各地多家實驗室都在嘗試確定EDRF本質(zhì),后續(xù)研究驚奇地發(fā)現(xiàn)EDRF與NO具有極大相似性。
首先,EDRF和NO生理功能相似性。二者都會導(dǎo)致血管擴張,并且都通過激活鳥苷酸環(huán)化酶生成cGMP實現(xiàn)。這一點和其他證據(jù)促使穆拉德于1986年提出,EDRF就是內(nèi)源NO。
其次,EDRF和NO化學(xué)性質(zhì)相似性。兩種物質(zhì)半衰期都極短,并且都可影響血紅素光譜吸收,且影響結(jié)果分毫不差,而測試的其他任何分子都不具備如此神奇效果。基于此,穆拉德認(rèn)定EDRF就是NO。
1986年,弗奇戈特和加州大學(xué)洛杉磯分校的路易斯·伊格納羅(Louis Ignarro)在第四屆舒張血管機制國際研討會上同時報道這項發(fā)現(xiàn),遺憾的是大多數(shù)人并不相信他們的結(jié)果。但隨后越來越多的證據(jù)支持EDRF和NO二者的一致性,科學(xué)界逐漸接受了這一事實。
1988年,研究人員證明精氨酸是體內(nèi)NO生成的原料;1990年,研究人員在大腦中獲得催化NO生成的酶,稱為大腦NO合酶(bNOS),又稱NOS-1;1991年,進一步發(fā)現(xiàn)內(nèi)皮細(xì)胞NO合酶(eNOS),又稱NOS-3;在巨噬細(xì)胞中發(fā)現(xiàn)誘導(dǎo)型NOS(iNOS),又稱NOS-2。至此,三種NOS鑒定完畢,它們發(fā)揮不同生理功能,分別為舒張血管、抵抗感染和神經(jīng)保護。至此,體內(nèi)存在NO已成科學(xué)事實。
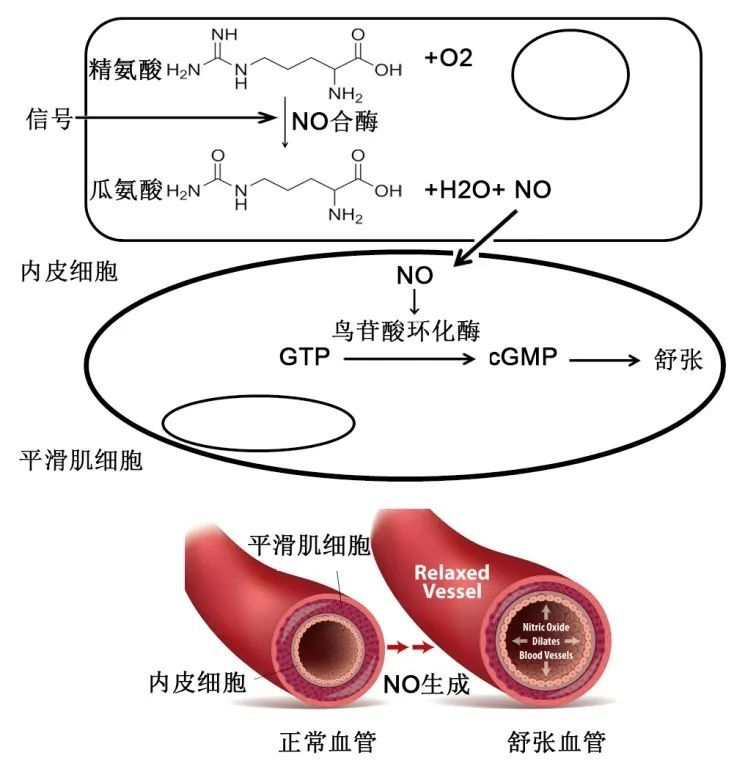
體內(nèi)NO生成
七
功成名就
后續(xù)研究發(fā)現(xiàn)NO遠比想象中更為重要,它參與了廣泛的生物學(xué)過程,特別是作為動物體內(nèi)第一種氣體信號分子,為其他氣體信號分子如CO、H2S等發(fā)現(xiàn)和研究提供重要思路,1992年,NO被《科學(xué)》雜志評為年度明星分子。
隨著NO重要性日益顯現(xiàn),穆拉德也開始獲得一系列科學(xué)獎勵。1996年,穆拉德和弗奇戈特分享拉斯克基礎(chǔ)醫(yī)學(xué)獎;1998年,他們又和伊格納羅分享諾貝爾生理學(xué)或醫(yī)學(xué)獎。諾貝爾評獎委員會認(rèn)為,穆拉德有關(guān)NO和cGMP的研究發(fā)現(xiàn)不僅詮釋了一類古老藥物的工作原理,而且還為許多生理現(xiàn)象理解和疾病治療提供新思路。現(xiàn)在已知,NO在炎癥形成、血液循環(huán)、組織發(fā)育、平滑肌舒張和長期記憶等過程均發(fā)揮重要作用,在心臟病、中風(fēng)、癌癥、肺部高血壓等臨床應(yīng)用方面也具有重要潛力,如吸入NO治療患有持續(xù)性肺動脈高壓的早產(chǎn)兒。
八
老而彌堅
穆拉德一直摯愛著自己的科研事業(yè),執(zhí)著于揭示生命奧秘并期望能造福于人類。
1970年到1981年間,穆拉德在弗吉尼亞大學(xué)工作,于1975年成為學(xué)校最年輕教授之一,1971年成為臨床研究中心主任和1973年臨床藥理學(xué)主任;他建立了一個臨床和基礎(chǔ)相結(jié)合的研究團隊,取得科研成果的同時還培養(yǎng)了一大批青年人,他們成為科學(xué)發(fā)展的后備力量。1981年,穆拉德加入斯坦福大學(xué),直到1989年。
為了能將科研成果更好轉(zhuǎn)化,穆拉德于1988年加入雅培公司,擔(dān)任副總裁,在隨后的4年間開展新藥研發(fā)和臨床試驗工作,大膽嘗試一些疾病新療法,遺憾的是未達自己預(yù)期而離職。1993年,穆拉德親自成立一家生物技術(shù)公司,擔(dān)任總裁兼首席執(zhí)行官,在未能籌備到足夠資金而自己的投入又花費殆盡的情況下,創(chuàng)業(yè)中道崩殂。
1997年,穆拉德重回學(xué)術(shù)界,加入得克薩斯大學(xué)休斯敦分校,再次開展基礎(chǔ)研究。獲得諾貝爾獎后,穆拉德日程變得繁忙起來,需要參與多種社交活動,因此有機會推廣自己的學(xué)術(shù)理念。穆拉德精力旺盛,在多家單位開展廣泛的研究,2011年時仍加入華盛頓大學(xué)工作。
2023年9月4日,穆拉德在加利福尼亞州門洛帕克去世,享年86歲。
穆拉德科研生涯完美詮釋了生命過程需要“NO(一氧化氮)”,而科研過程更需要 “NO(不)”。不拘泥傳統(tǒng)思維、勇于向陳舊觀念挑戰(zhàn)應(yīng)是偉大科學(xué)家的先天因素。
主要參考文獻
[1] 郭曉強.內(nèi)皮細(xì)胞舒血管因子的發(fā)現(xiàn)者——弗奇戈特.科學(xué)(上海), 2010, 62(3):45-48.
[2] Sharina I, Martin E. Ferid Murad (1936-2023).Science, 2023, 382(6670):519.
[3] Murad F. Some highlights of a 47 year career in research. Cell Mol Life Sci, 2005, 62(1):1-3.
[4] Murad F. Discovery of some of the biological effects of nitric oxide and its role in cell signaling. Biosci Rep, 2004, 24(4-5):452-474.
[5] Steinhorn BS, Loscalzo J, Michel T. Nitroglycerin and Nitric Oxide--A Rondo of Themes in Cardiovascular Therapeutics. N Engl J Med, 2015, 373(3):277-280.
[6] Mittal CK, Kimura H, Murad F. Requirement for a macromolecular factor for sodium azide activation of guanulate cyclase. J Cyclic Nucleotide Res, 1975, 1(6):261-269.
[7] Kimura H, Mittal CK, Murad F. Activation of guanylate cyclase from rat liver and other tissues by sodium azide. J Biol Chem, 1975, 250(20):8016-8022.
[8] Katsuki S, Arnold W, Mittal C, Murad F. Stimulation of guanylate cyclase by sodium nitroprusside, nitroglycerin and nitric oxide in various tissue preparations and comparison to the effects of sodium azide and hydroxylamine. J Cyclic Nucleotide Res, 1977, 3(1):23-35.
[9] Katsuki S, Arnold WP, Murad F. Effects of sodium nitroprusside, nitroglycerin, and sodium azide on levels of cyclic nucleotides and mechanical activity of various tissues. J Cyclic Nucleotide Res, 1977, 3(4):239-247.
[10] Murad F. Cyclic guanosine monophosphate as a mediator of vasodilation. J Clin Invest, 1986, 78(1):1-5.

特 別 提 示
1. 進入『返樸』微信公眾號底部菜單“精品專欄“,可查閱不同主題系列科普文章。
2. 『返樸』提供按月檢索文章功能。關(guān)注公眾號,回復(fù)四位數(shù)組成的年份+月份,如“1903”,可獲取2019年3月的文章索引,以此類推。
版權(quán)說明:歡迎個人轉(zhuǎn)發(fā),任何形式的媒體或機構(gòu)未經(jīng)授權(quán),不得轉(zhuǎn)載和摘編。轉(zhuǎn)載授權(quán)請在「返樸」微信公眾號內(nèi)聯(lián)系后臺。
來源: 返樸
內(nèi)容資源由項目單位提供


 科普中國公眾號
科普中國公眾號
 科普中國微博
科普中國微博

 幫助
幫助
 返樸
返樸 
