
前言概述
/ CONTENTS
學(xué)科新知聚焦業(yè)內(nèi)權(quán)威專家,從學(xué)科發(fā)展的高度全面梳理、深入解讀腫瘤醫(yī)學(xué)各領(lǐng)域的國內(nèi)外研究現(xiàn)狀與進(jìn)展,為醫(yī)護(hù)以及科研人員立體勾勒惡性腫瘤領(lǐng)域的最新研究進(jìn)展,賦能臨床科研和學(xué)術(shù)推廣,為醫(yī)學(xué)研究者搭建一個共享知識、交流經(jīng)驗(yàn)的平臺,推動腫瘤醫(yī)學(xué)領(lǐng)域的國際化合作與發(fā)展。
本期學(xué)科新知分享的是重慶醫(yī)科大學(xué)附屬第一醫(yī)院王利教授對自體造血干細(xì)胞移植(auto-HSCT)序貫CAR-T細(xì)胞治療在彌漫性大B細(xì)胞淋巴瘤(DLBCL)中的臨床實(shí)踐以及未來展望的精彩解讀。
1
DLBCL治療中的“利器”
彌漫性大B細(xì)胞淋巴瘤是一種來源于成熟B細(xì)胞的侵襲性腫瘤,是最常見的非霍奇金淋巴瘤類型,約占全部非霍奇金淋巴瘤的25%~50%。DLBCL臨床異質(zhì)性大,2016年WHO分類共列出19種大B細(xì)胞淋巴瘤亞型,不同亞型具有不同的臨床特征、遺傳學(xué)改變及治療反應(yīng)[1]。R-CHOP(利妥昔單抗+環(huán)磷酰胺+阿霉素+長春新堿/長春地辛+潑尼松)是目前治療DLBCL的標(biāo)準(zhǔn)方案,然而仍有30%~40%的患者經(jīng)過初次治療后出現(xiàn)復(fù)發(fā)或發(fā)展成難治型[2]。
根據(jù)臨床治療結(jié)果將耐藥復(fù)發(fā)大致分成3型:(1)初始治療時即表現(xiàn)為藥物抵抗(EMDR)。這種類型叫原發(fā)基因抵抗,與基因異常表達(dá)及循環(huán)易位有關(guān)。(2)獲得性EMDR是化療后發(fā)展而來,EMDR性亞克隆細(xì)胞的出現(xiàn)導(dǎo)致了利妥昔單抗及蒽環(huán)類藥物為基礎(chǔ)的化療失敗。(3)腫瘤微環(huán)境黏附介導(dǎo)藥物抵抗,是由于DLBCL的淋巴瘤細(xì)胞與正常間質(zhì)細(xì)胞相互作用而產(chǎn)生[2]。
對于復(fù)發(fā)難治性DLBCL的患者,可選擇挽救化療、造血干細(xì)胞移植、新藥治療、免疫治療。挽救化療的目的是在干細(xì)胞移植治療之前最大限度地減少瘤細(xì)胞[3]。挽救化療方案包括R-DHAP方案(利妥昔單抗+地塞米松+大劑量阿糖胞苷+順鉑),R-GDP方案(利妥昔單抗+吉西他濱+順鉑+地塞米松)或R-ICE方案(利妥昔單抗+異環(huán)磷酰胺+卡鉑+依托泊苷)等[2]。依照PARMA研究,auto-HSCT相比于傳統(tǒng)挽救化療,具有更好的5年生存率,在二線治療中具有極大優(yōu)勢[4]。三線挽救化療后應(yīng)用auto-HSCT較未做移植的患者也會獲得較長的生存期[5]。在指南中也推薦auto-HSCT用于部分侵襲性淋巴瘤亞型的一線鞏固治療和復(fù)發(fā)/難治性淋巴瘤的挽救性治療[6,7]。整體治療流程包括干細(xì)胞動員及采集、移植前預(yù)處理、干細(xì)胞回輸、合并癥管理、植入情況評估。此外,在行auto-HSCT前,需要對患者進(jìn)行移植前誘導(dǎo)及療效評估。目前造血干細(xì)胞動員方案主要包括:化療聯(lián)合細(xì)胞因子方案、單獨(dú)應(yīng)用細(xì)胞因子方案和含趨化因子受體CXCR4拮抗劑動員方案[8]。
然而,高齡、基礎(chǔ)疾病較多者并不適用此方法,新藥或者免疫治療則成為這類患者的優(yōu)選方案。在新藥的探索中,關(guān)于利妥昔單抗聯(lián)合苯達(dá)莫司汀(RB)治療的回顧性分析顯示其在高齡及基礎(chǔ)疾病較多患者中有效率較高,相關(guān)毒性可控。有關(guān)來那度胺的回顧性研究中,顯示其在非生發(fā)中心型(non-GCB)中CR率32%,PR率33%。且其不良反應(yīng)少并可控[2]。來那度胺聯(lián)合化療(R-ICE方案),在治療2個周期后,評價CR率60%,PR率13%[2]。基于NP30179的研究結(jié)果,格非妥單抗(CD20×CD3雙特異性抗體)可早期實(shí)現(xiàn)較高的完全緩解率,中位隨訪18.2個月,獨(dú)立評審委員會評估CR率(最佳整體緩解[BOR])為40%,客觀緩解率(ORR)為52%,多數(shù)患者(68%)仍維持CR,中位CR持續(xù)時間(DoCR)為26.9個月,不論患者何時達(dá)到CR,18個月時約70%患者處于緩解狀態(tài),18個月的總生存(OS)率為41%[9]。維泊妥珠單抗作為一種靶向CD79b的抗體偶聯(lián)藥物,在DLBCL的治療領(lǐng)域也開啟了新的篇章,Pola-R-CHP(維泊妥珠單抗聯(lián)合利妥昔單抗、環(huán)磷酰胺、多柔比星和潑尼松)方案將2年無進(jìn)展生存率提升至76.7%,疾病進(jìn)展、復(fù)發(fā)或死亡的相對風(fēng)險降低27%,且足療程治療比例更高,發(fā)生致劑量降低的不良事件更少[10]。
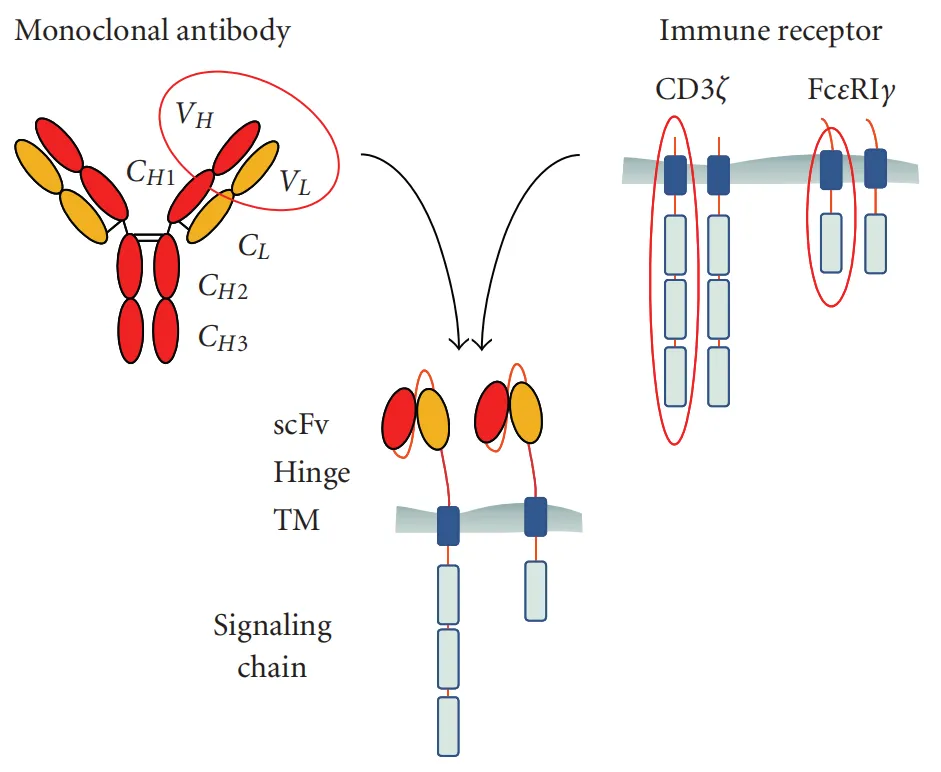
在免疫治療方面,除傳統(tǒng)的免疫檢查點(diǎn)抑制劑外,嵌合抗原受體T細(xì)胞免疫療法(CAR-T)的出現(xiàn)打開了腫瘤治療的新的大門。簡言之,CAR-T治療即是通過基因工程技術(shù),人為地在正常T細(xì)胞中嵌合特定抗原受體(CAR),使得T細(xì)胞行使特異的殺傷功能。CAR分子包括三個主要部分:胞外域、跨膜域和胞內(nèi)域。胞外結(jié)構(gòu)域:負(fù)責(zé)結(jié)合靶抗原和靶細(xì)胞;跨膜結(jié)構(gòu)域:將CAR錨定在免疫細(xì)胞上;穩(wěn)定CAR結(jié)構(gòu);與其他膜蛋白結(jié)合;胞內(nèi)結(jié)構(gòu)域:指CD3和(或)其他T細(xì)胞激活所需的共刺激信號因子,主要負(fù)責(zé)激活免疫細(xì)胞。
CAR-T細(xì)胞療法是基于患者自身免疫系統(tǒng)的個性化治療方式,每例治療都是針對個體定制,開創(chuàng)了精準(zhǔn)醫(yī)療的新時代。在復(fù)發(fā)難治性DLBCL中,CAR-T細(xì)胞治療的出現(xiàn)是一個里程碑事件,其在淋巴瘤治療體系中發(fā)揮了重大的作用,尤其是B細(xì)胞淋巴瘤的治療效果再上一個臺階。CAR-T細(xì)胞療法的有效率可高達(dá)52%~82%,完全緩解率可達(dá)40%~54%。然而,在臨床應(yīng)用中,一些身體有大包塊、病情進(jìn)展迅速的患者采用CAR-T治療后的效果并不盡如人意。對于累及中樞、睪丸、乳腺等免疫豁免器官的淋巴瘤,一旦復(fù)發(fā)難治使用CAR-T治療效果十分有限。整體來看,單用CAR-T治療也僅能讓40%~50%難治、復(fù)發(fā)的淋巴瘤患者得到緩解。
2
自體造血干細(xì)胞移植與CAR-T的“合奏曲”
此項(xiàng)由中國學(xué)者全球新創(chuàng)的療法相關(guān)的開創(chuàng)性臨床研究的療效結(jié)果于2021年8月在全球血液學(xué)核心期刊《移植與細(xì)胞治療》中發(fā)表。淋巴瘤具有介于白血病和實(shí)體瘤之間的特征,其復(fù)雜的腫瘤免疫抑制微環(huán)境(TME)會限制CAR-T功能,而輸注CAR-T細(xì)胞之前進(jìn)行強(qiáng)預(yù)處理清淋方案可破壞TME,能夠有效增強(qiáng)CAR-T細(xì)胞的功能和增殖。在auto-HSCT的強(qiáng)預(yù)處理方案后,免疫抑制性TME會降低,使得腫瘤負(fù)荷明顯下降。在造血重建期間給予CAR-T細(xì)胞治療,可以根除移植后的殘余疾病,從而降低復(fù)發(fā)率。
隨后,中國學(xué)者也在全球首次提出自體造血干細(xì)胞移植聯(lián)合CAR-T能夠使疾病處于進(jìn)展期和有中樞侵犯的患者獲得長期治愈的可能。研究結(jié)果發(fā)表在國際權(quán)威雜志《血液腫瘤》中,獲得國內(nèi)外同行的一致認(rèn)可,引發(fā)廣泛關(guān)注,并在多家著名的血液病中心得以證實(shí)其療效及安全性。因此,對于高危的復(fù)發(fā)難治性彌漫大B細(xì)胞淋巴瘤,或者是有中樞、卵巢、睪丸等特殊部位侵犯,以及有高危遺傳因素的淋巴瘤患者,采用自體移植聯(lián)合CAR-T的治療方式則會取得更好的療效。
2021年美國血液學(xué)年會一項(xiàng)關(guān)于伴有不良預(yù)后的TP53突變高危復(fù)發(fā)/難治性非霍奇金淋巴瘤患者進(jìn)行單獨(dú)CAR-T治療或聯(lián)合ASCT治療的研究顯示,伴TP53突變的單純CAR-T治療組患者估計(jì)24個月的無進(jìn)展生存率和OS率為48.4%和56.3%,而CAR-T聯(lián)合ASCT治療組患者的無進(jìn)展生存率與OS率分別提升至77.5%和89.3%,生存率得到了顯著提高。在2022年ASCO年會上,一項(xiàng)關(guān)于auto-HSCT聯(lián)合CD30 CAR-T細(xì)胞輸注在復(fù)發(fā)難治性CD30+淋巴瘤患者中,所有患者在數(shù)據(jù)截止日期時(2022年1月31日)均保持緩解,并且仍然存活,未出現(xiàn)疾病復(fù)發(fā)或進(jìn)展。此外,在入組時疾病穩(wěn)定/進(jìn)展的患者也均保持緩解。2024年EBMT年會上,一項(xiàng)在復(fù)發(fā)難治性中樞神經(jīng)系統(tǒng)淋巴瘤中的研究表明采取auto-HSCT聯(lián)合CAR-T細(xì)胞治療可將患者3個月的客觀緩解率和完全緩解率分別提高到84.4%和82.2%。患者的中位無進(jìn)展生存期也延長到43.07個月,1年OS率和無進(jìn)展生存率分別為100%和74.7%。
Auto-HSCT與CAR-T細(xì)胞的聯(lián)合應(yīng)用,一方面利用auto-HSCT恢復(fù)患者的免疫功能,另一方面通過CAR-T精準(zhǔn)打擊殘留病灶,“雙劍合璧”共同增強(qiáng)治療效果。此聯(lián)合治療策略通過各自優(yōu)勢疊加,突破傳統(tǒng)治療的局限,實(shí)現(xiàn)更深層次的腫瘤清除。
3
Auto-HSCT與CAR-T攜手,中國智慧共助患者“破繭新生”
Auto-HSCT聯(lián)合CAR-T治療不僅在臨床實(shí)驗(yàn)中取得了優(yōu)異的成績,在實(shí)際的臨床應(yīng)用中,Auto-HSCT聯(lián)合CAR-T治療也為淋巴瘤患者的長期生存帶來希望。
重慶醫(yī)科大學(xué)附屬第一醫(yī)院就診的罹患復(fù)發(fā)難治彌漫大B細(xì)胞淋巴瘤的陳先生在進(jìn)行自體造血干細(xì)胞移植續(xù)貫CAR-T細(xì)胞順利出院。陳先生曾因“咽部新生物1月”被診斷為彌漫大B細(xì)胞淋巴瘤(GCB型,Ⅱ期A組,IPI 0分,低危組)。盡管在規(guī)律一線治療4個療程后達(dá)到完全緩解,但在繼續(xù)完成后續(xù)治療中再次出現(xiàn)咽喉部及頸部包塊。給予二線治療措施病情無法控制,咽喉部包塊進(jìn)行性增大,導(dǎo)致他出現(xiàn)吞咽困難及呼吸困難。患者咽部新生物在規(guī)律治療中反復(fù)進(jìn)展,腫瘤生長極其迅速,同時伴有高Ki-67、TP53突變等多個不良預(yù)后因素。通過“MDT to HIM”的理念,整合全科專家,決定為患者采用自體造血干細(xì)胞移植序貫CAR-T細(xì)胞治療。從醫(yī)療組、實(shí)驗(yàn)室、護(hù)理團(tuán)隊(duì)三方面一同出發(fā),聚焦腫瘤的“診-治-康”。患者造血重建迅速,腫大的包塊消失。沒有嚴(yán)重的感染、出血以及細(xì)胞因子釋放綜合征和神經(jīng)毒性的發(fā)生,最終順利出院。
童先生,同樣就診于重慶醫(yī)科大學(xué)附屬第一醫(yī)院,在進(jìn)行auto-HSCT聯(lián)合CAR-T治療后也重獲新生。最初,患者無明顯誘因出現(xiàn)咳嗽、咳黃膿痰,院內(nèi)行PET-CT提示:右肺門處巨大軟組織密度腫塊影(13.0×6.8cm),形態(tài)不規(guī)則,密度欠均勻,周圍伴阻塞性炎性改變,代謝活性增高(SUVmax值為22.9)Deauville評分5分;雙肺多發(fā)軟組織密度結(jié)節(jié),代謝活性增高,Deauville評分5分,病理提示:結(jié)合免疫組化和組織形態(tài),被診斷為彌漫大B細(xì)胞淋巴瘤(診斷:non-GCB型,Ⅳ期B組,IPI評分3分,中高危組)。腫瘤的基因二代測序檢測出:TP53(52.7%)、CCND3(62.48%)、KMT2C(40.92%)、NCOR2(87.55%)等,在規(guī)律一線治療Pola-RCHP方案3個療程后;右肺病變范圍較前明顯縮小,代謝活性較前明顯減低(SUVmax值為5.2),Deauville評分3分;雙肺多發(fā)實(shí)性小結(jié)節(jié),較大者位于右肺上葉尖段,較大者代謝活性輕度增高,較大者Deauville評分3分,余者評分1分,療效評估達(dá)到PR,后順利進(jìn)行第四次免疫化療,后成功進(jìn)行動員采集造血干細(xì)胞,采集治療達(dá)標(biāo),在進(jìn)行第5次免疫化療時提示腫瘤進(jìn)展,6次免疫化療后成功行造血干細(xì)胞移植,序貫CAR-T細(xì)胞治療,患者順利出院。
4
未來展望
臨床研究的亮眼結(jié)果和臨床應(yīng)用的成功案例為未來自體造血干細(xì)胞移植聯(lián)合CAR-T細(xì)胞治療的更廣泛的實(shí)施帶來美好的期待。然而,作為一項(xiàng)新的治療手段,理想的順序和組合還有待更多的臨床試驗(yàn)進(jìn)行闡明。此外,部分患者對特定療法有反應(yīng),部分患者則出現(xiàn)抵抗效果,以及何種患者可從治療中獲益,這些仍是尚未撥開的迷霧。因此,需要更深入地了解DLBCL的生物學(xué)以及新藥或者新的治療法方如何影響其生物學(xué)功能。基于此類問題的出發(fā)有望新的治療組合的研發(fā)以及最優(yōu)治療順序的進(jìn)行。如此這般,才能夠?yàn)閺V大的彌漫性大B細(xì)胞淋巴瘤帶來福音。

參考文獻(xiàn)(向上滑動閱覽)
[1]中華人民共和國國家衛(wèi)生健康委員會.彌漫性大B細(xì)胞淋巴瘤診療指南(2022 年版).http://www.nhc.gov.cn/
[2]竇征岳, 夏冰, 張翼鷟. 復(fù)發(fā)難治性彌漫大B細(xì)胞淋巴瘤研究進(jìn)展 [J] . 白血病·淋巴瘤,2017,26 (9): 562-566. DOI: 10.3760/cma.j.issn.1009-9921.2017.09.015
[3]Hernandez-IlizaliturriFJ, CzuczmanMS. Therapeutic options in relapsed or refractory diffuse large B-cell lymphoma. Part 1. current treatment approaches[J]. Oncology(Williston Park),2009,23(6):546-553.
[4]FarooqU, LaportGG. Recent progress:hematopoietic cell transplant for diffuse large B-cell lymphoma[J]. Leuk Lymphoma,2015,56(7):1930-1937. DOI:10.3109/10428194.2014.975803.
[5]Van Den NesteE, SchmitzN, MounierN,et al. Outcome of patients with relapsed diffuse large B-cell lymphoma who fail second-line salvage regimens in the International CORAL study[J]. Bone Marrow Transplant,2016,51(1):51-57. DOI:10.1038/bmt.2015.213.
[6]KANATE A S, MAJHAIL N S, SAVANI B N, et al. Indications for hematopoietic cell transplantation and immune effector cell therapy: guidelines from the American Society for Transplantation and Cellular Therapy[J]. Biol Blood Marrow Transplant, 2020, 26(7): 1247-1256.
[7]NCCN. NCCN Clinical Practice Guidelines in Oncology[M]. B-cell lymphomas, version 5, September 22, 2021.
[8]中華醫(yī)學(xué)會血液學(xué)分會. 淋巴瘤自體造血干細(xì)胞動員和采集中國專家共識(2020年版) [J] . 中華血液學(xué)雜志, 2020, 41(12): 979-983. DOI: 10.3760/cma.j.issn.0253-2727.2020.12.002.
[9]Hutchings M, et al. Glofitamab monotherapy in patients with relapsed/refractory (R/R) large B-cell lymphoma (LBCL):extended follow-up and landmark analyses from a pivotal phase II study. 2023 ASCO Poster 7550; 2023 EHA. Poster 1129; 2023 ICML Oral 95.
[10]Tilly H, Morschhauser F, Sehn LH, et al. Polatuzumab Vedotin in Previously Untreated Diffuse Large B-Cell Lymphoma. N Engl J Med. 2022;386(4):351-363. doi:10.1056/NEJMoa2115304
[11]隗佳, 肖敏, 周劍峰, 等. 2021ASH. Oral 94.
來源: CACA前沿


 科普中國公眾號
科普中國公眾號
 科普中國微博
科普中國微博

 幫助
幫助
 樂問醫(yī)學(xué)
樂問醫(yī)學(xué) 