高血糖會損傷人的血管、削弱免疫力,阻礙傷口修復。通常,糖尿病患者的傷口也很難愈合,甚至面臨截肢風險,嚴重影響患者生活質量,也給家庭和社會帶來沉重的負擔。
“我們新近開發的一種源自蝸牛黏液的糖胺聚糖類新型生物材料,或許能為糖尿病足潰瘍帶來轉機!”8月13日,中國科學院昆明植物研究所研究員吳明一告訴科技日報記者。
原來,吳明一帶領團隊開發出新型仿細胞外基質結構凝膠貼片,通過“抗菌—抗炎—促再生”三重機制,為糖尿病足潰瘍治療提供了全新方案。這項研究成果以研究論文全文形式,發表在國際期刊《碳水化合物聚合物》上,為全球數億糖尿病患者帶來福音。
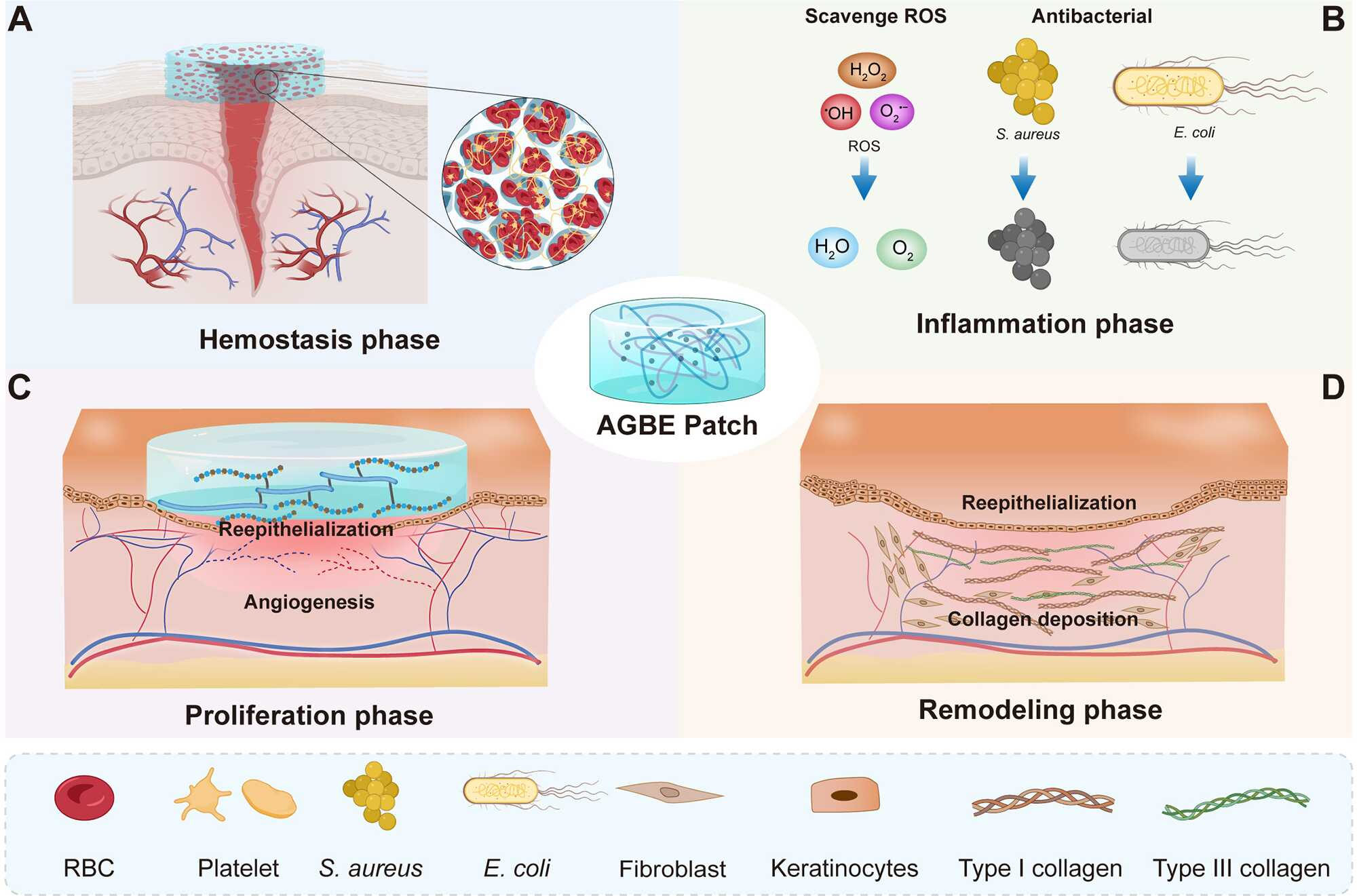
糖尿病足潰瘍:沉默的“肢體殺手”
糖尿病足潰瘍,是糖尿病最嚴重的慢性并發癥之一。全球約4000萬至6000萬人受其困擾,患者年死亡率高達22%,超過許多癌癥。
用傳統治療手段治療該病,通常面臨兩大困境:一方面,抗生素濫用導致耐藥菌滋生,50%以上患者對現有療法無響應;另一方面,高血糖環境下,傷口長期處于氧化應激和慢性炎癥狀態,表皮再生能力幾乎停滯。
“就像在鹽堿地里種莊稼,細菌不斷‘搗亂’,傷口微環境的‘土壤’又板結缺氧,再好的種子也難以發芽。”吳明一研究員形象地比喻。臨床數據顯示,糖尿病足潰瘍患者的截肢風險是普通人的25倍,且復發率超過60%。
創新靈感往往來自大自然。
長期以來,吳明一團隊聚焦面向心腦血管、糖尿病及其并發癥等重大疾病的臨床需求,開展天然聚糖的純化制備、結構解析、藥理活性以及成藥性評價等新藥發現相關的基礎研究。他們注意到,蝸牛爬行時分泌的黏液具有驚人的修復能力——即使在粗糙巖石上劃傷,也能快速愈合。通過成分分析,發現黏液中的核心活性物質是一種特殊的糖胺聚糖(AFG),其結構與人體細胞外基質中的糖胺聚糖高度相似。
“細胞外基質就像細胞的‘搖籃’,調控細胞的增殖、遷移等生命活動。”論文第一作者鄧拓博士解釋。受此啟發,團隊將蝸牛糖胺聚糖與明膠通過共價鍵交聯,構建出類似人體細胞外基質的三維凝膠網絡。
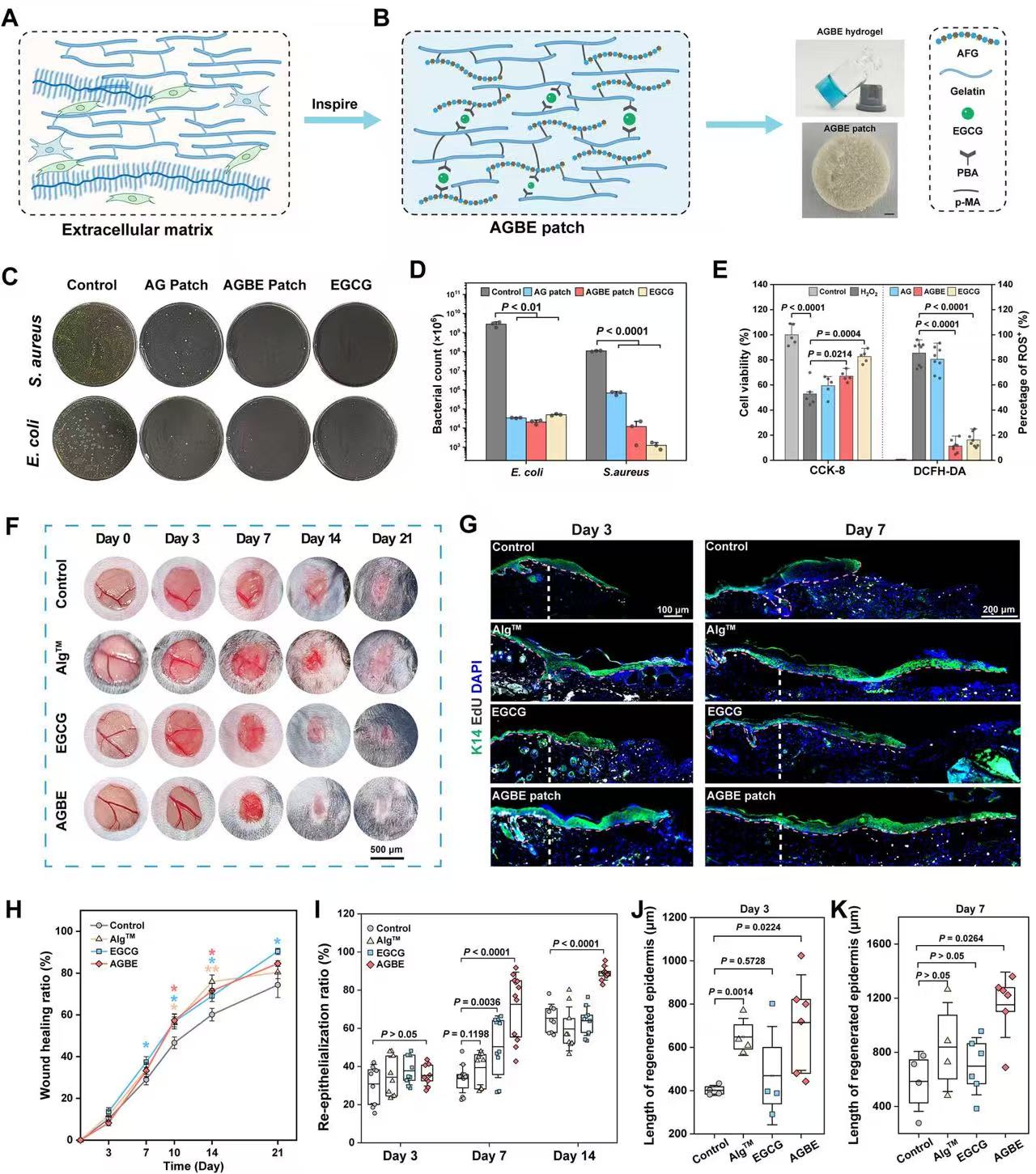
三重機制破解糖尿病足愈合難題
在創新研發過程中,研究團隊引入天然植物綠茶中的茶多酚EGCG,通過動態硼酸酯鍵技術,將其“錨定”在凝膠中,制備出兼具多重功能的抗菌、抗氧化、抗炎以及促進組織再生的凝膠貼片。
這一設計,其實暗藏著智能“機關”。當傷口局部葡萄糖濃度升高時,硼酸酯鍵會斷裂并釋放EGCG,實現“按需給藥”;而當血糖趨于穩定時,藥物釋放自動減緩,避免了傳統給藥方式的副作用。
在實驗室中,抗菌、抗氧化、抗炎以及促進組織再生的凝膠貼片展現出“全能選手”般的表現。在體外實驗顯示,其對金黃色葡萄球菌和大腸桿菌的殺滅率達99.9%,效果媲美臨床抗生素,但不存在耐藥性風險;同時,它能清除80%以上的活性氧自由基,為傷口細胞創造“清新環境”。而在糖尿病小鼠模型中,貼片組傷口7天表皮再生率達72.6%,是生理鹽水組的2倍多,且膠原纖維排列與正常皮膚幾乎一致。
“最關鍵的是它能‘安撫’過度活躍的免疫系統。”團隊成員、論文第一作者之一的李軒介紹,這種凝膠貼片可使傷口炎癥因子水平下降50%以上,打破“炎癥—組織壞死”的惡性循環。在感染模型中,貼片還能阻止細菌定植,避免傷口惡化。
這項研究為何能脫穎而出?國際期刊審稿人評價其“將天然產物與仿生材料完美結合”,并具有三大創新點:一是材料創新,將蝸牛糖胺聚糖用于創面修復,避免了傳統肝素類藥物的出血風險;其次是設計的智慧,用動態共價鍵實現“智能釋藥”,解決了EGCG易氧化、生物利用度低的難題;三是能同時調控感染、炎癥、再生三大病理環節,直擊糖尿病傷口的核心痛點。
“我們期待通過后續持續研究,使這款‘仿生創可貼’讓更多患者獲益。”吳明一研究員介紹,這一成果未來還可拓展至壓瘡、燒傷等難愈合創面治療,甚至開發成家用護理產品。
來源: 科技日報


 科普中國公眾號
科普中國公眾號
 科普中國微博
科普中國微博

 幫助
幫助
 北京科協
北京科協 